
Nitrógeno y fósforo, los macronutrientes agronómicos por excelencia
Creo que la mayoría de la gente conocemos, de una manera u otra, características de los elementos químicos de los que vamos a hablar en esta publicación: el nitrógeno (N) y el fósforo (P). El nitrógeno en su forma gaseosa (N2) forma parte de la composición del aire atmosférico o incluso lo conocemos en otras de sus formas típicas, el amoníaco (NH3), ya sea como gas o como disolución líquida (en caso como amonio NH4+). Mientras que el fósforo participa en funciones vitales de los seres vivos, además de ser uno de los componentes principales de las moléculas de ARN y ADN y de utilizarse para almacenar y transportar energía en forma de adenosín trifosfato (ATP). Pues bien, hoy en esta entrada vamos a profundizar en por qué estos dos elementos son también importantes para otros temas relacionados con los seres humanos y su desarrollo, expondremos cuál es la importancia del nitrógeno (N) y fósforo (P) como nutrientes agronómicos y cómo se relacionan éstos con el concepto de Economía Circular (un concepto de rabiosa actualidad en los últimos años). Por lo tanto, en adelante cuando en esta publicación estemos hablando de nutrientes, siempre estará enfocado desde un punto de vista agronómico y no desde un punto de vista alimentario del propio ser humano. ¡Empezamos!
Tanto el N, como el P junto con el potasio (K), forman el grupo de los macronutrientes agronómicos, éstos son los tres principales macroelementos que las plantas o cultivos necesitan incorporar para su crecimiento. Así, en la mayoría de las ocasiones los fertilizantes que se sintetizan y se utilizan hoy en día en la agricultura presentan una composición importante de dichos elementos (se suele hablar del contenido NPK en dichos productos).
Lo primero que debemos preguntarnos es ¿cómo se sintetizan dichos fertilizantes?
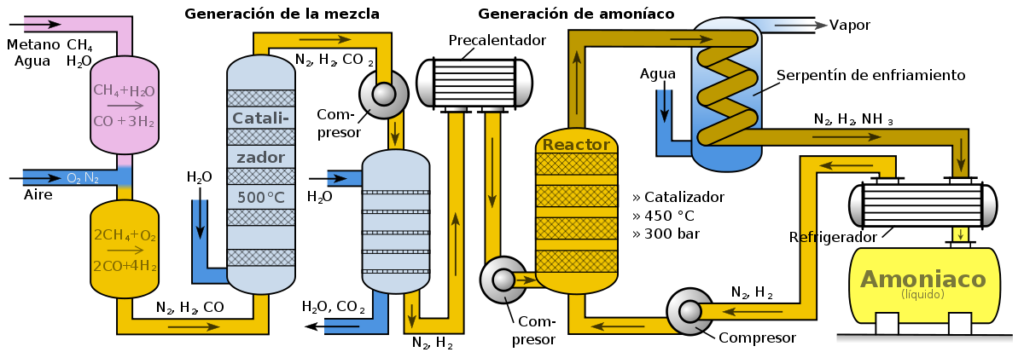
Casi la totalidad del N utilizado en la formulación de fertilizantes es obtenida a partir de la síntesis de amoníaco, el procedimiento clásico de la obtención de amoníaco es el proceso Haber-Bosch. Posteriormente, el amoniaco obtenido mediante Haber-Bosch, se oxida para dar lugar al ácido nítrico (HNO3) y a partir de éste se pueden obtener los principales fertilizantes minerales, sintetizados a partir de nitrato de amonio [(NH4)NO3]. La otra fuente principal de N para la síntesis de fertilizantes es la urea [(NH2)2CO]. En lo que respecta al fósforo, la principal materia prima para su utilización en fertilizantes es la apatita, se trata de un conjunto de minerales obtenidos a través de la extracción de la roca fosfórica mineral. Por lo tanto, lo primero de lo que podemos darnos cuenta es que, en ambos casos, el origen de N y P para la obtención de los fertilizantes tradicionales, es un origen no renovable.
A este factor hay que incluir otro con una gran importancia, y ese no es otro que el aumento de la población mundial. De acuerdo con las previsiones de Naciones Unidas (ONU), la población mundial alcanzará los 8.600 millones en 2030 y los 9.800 millones en 2050. Con lo que queda patente, que estos hechos darán lugar a un importante incremento de presión de la industria alimentaria, que estará abocada a aumentar su producción, lo cual conlleva prácticas agrícolas más intensivas y por tanto un aumento del uso de la tierra y del consumo del agua, la energía y los fertilizantes tradicionales no renovables. Otro hecho preocupante de este escenario es que los países de la Unión Europea (UE), son tremendamente dependientes de las importaciones de estos compuestos que actúan como materias primas para los fertilizantes. Para que nos hagamos una idea, la UE importa alrededor del 30% del N, más del 60% del P y el 70% del K del total de nutrientes que se consumen como productos fertilizantes en sus países. Este asunto, es incluso más dramático para el caso del P, ya que cinco países en todo el mundo poseen el 90% de las reservas mundiales (China, Marruecos, Sudáfrica, Estados Unidos y la región de Jordania). Esto ha hecho que la UE haya clasificado al P como Materia Prima Crítica (COM(2017)490), ya que es crucial para el crecimiento de la propia UE, la competitividad y especialmente para una industria alimentaria sostenible.
Con todo este escenario queda claro que es necesario la búsqueda e introducción de fuentes de N y P alternativas y renovables, a la par que tecnologías novedosas para la obtención de productos fertilizantes sostenibles.
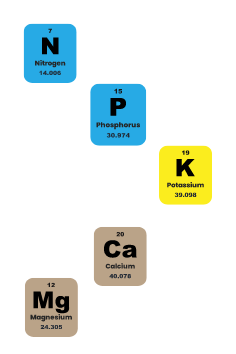
Y aquí es donde entra en escena, por un lado, la Economía Circular y por otro el concepto de recuperación de nutrientes. La recuperación de nutrientes es una de las principales líneas de investigación que llevamos desarrollando en los últimos años dentro del área de Economía Circular del Centro Tecnológico CARTIF. La recuperación de nutrientes consiste en el desarrollo de metodologías, técnicas y tecnologías que permiten obtener de materias primas sostenibles el N y el P que contienen y que estos elementos se encuentren en una forma conveniente y efectiva para su posterior utilización en la síntesis de bioproductos o fertilizantes sostenibles que puedan sustituir a los fertilizantes minerales tradicionales o en su defecto aumentar el componente renovable en la formulación de estos últimos. Es importante destacar que, aunque la recuperación de nutrientes se focalice principalmente en la recuperación de N y P, también se puede conseguir la recuperación de otros macro y micronutrientes agronómicos, como el K, el magnesio (Mg), el calcio (Ca), etc.
Y entonces, ¿qué materias primas o fuentes de origen renovable podemos utilizar para la recuperación de nutrientes?
Principalmente, la recuperación de nutrientes se centra en dos grupos; los residuos agroganaderos y las aguas residuales. Como residuos agroganaderos entendemos cualquier residuo generado directamente en la actividad agrícola o ganadera (estiércoles, purines, etc.), así como aguas residuales (tanto de origen urbano como origen industrial). Además, y relacionado con lo anterior también podrían utilizarse en la recuperación de nutrientes los residuos biológicos o subproductos obtenidos en el tratamiento de dichos residuos (un ejemplo claro sería los digestatos obtenidos del tratamiento de dichos residuos mediante digestión anaerobia o los fangos obtenidos en los procesos de tratamiento de aguas residuales en Estaciones Depuradoras de Aguas Residuales (EDARs), etc.).

Un aspecto importante a destacar es que las tecnologías de recuperación de nutrientes dependen en gran medida de las características de la materia prima que utilicemos para recuperar el N y el P y cómo se presente dicha materia prima (en estado sólido o líquido). Así, los métodos más sencillos de recuperación de nutrientes son el uso directo como fertilizante de residuos o subproductos sólidos como los fangos activos o los estiércoles y digestatos o el compostaje de éstos. Sin embargo, los aspectos logísticos (coste de transporte y la gestión del residuo, los cuales suelen contener gran humedad), pueden hacer inviable la rentabilidad del proceso. Al mismo tiempo, mediante la aplicación directa de los residuos no se realiza una fertilización efectiva y puede dar lugar a fenómenos de sobrefertilización los cuales pueden desembocar en fenómenos de eutrofización (por la acumulación del N y P presente en el suelo, el cual no ha podido ser asimilado por el cultivo y que posteriormente puede ser arrastrado por la lluvia o la escorrentía y finalmente depositarse e en acuíferos y masas de agua), con el consiguiente daño ambiental. Además, los residuos pueden contener cantidades significativas de contaminantes potencialmente peligrosos, que es necesario eliminar antes de su utilización como fertilizantes. Por esta razón, las tecnologías para el tratamiento de residuos para la recuperación de N y P son cada vez más populares. Existen distintas tecnologías para recuperar el N y el P de residuos líquidos, como los tratamientos biológicos, el stripping, la cristalización, la filtración por membranas, métodos termoquímicos (pirólisis y gasificación) o tratamientos físicos (concentración, secado, etc.).
Pero como todo ello se entiende mejor con un ejemplo, vamos a tratar de explicar uno de los procesos en lo que hemos investigado en CARTIF en alguno de nuestros proyectos.
Se trata de la recuperación de nutrientes a partir de la cristalización. La cristalización es una operación de separación frecuentemente utilizada en la Ingeniería Química, gracias a la cual se produce una purificación de los fluidos mediante la formación de sólidos, teniendo en cuenta la solubilidad de los productos que presentan interés para su separación. Así mediante la cristalización se puede conseguir recuperar N y P a partir de aguas residuales o residuos agroganaderos líquidos (fase líquida de los digestatos y estiércoles o purines) en forma de estruvita.
Pero, un momento, vayamos por partes ¿qué es la estruvita?

La estruvita es una sal (mineral ortofosfato) que contiene magnesio, amonio y fosfato en concentraciones molares iguales, concretamente, la estruvita en forma de fosfato de magnesio y amonio hexahidratado presenta la siguiente fórmula molecular MgNH4PO4·6H20. La cristalización de estruvita ocurre con facilidad cuando se dan las condiciones idóneas (presencia de una concentración importante de Mg, N y P, pH,etc.) De hecho, la estruvita en la década de los sesenta, ganó la atención del público como resultado de la obstrucción de tuberías en EDARs, en las cuales cristalizaba de forma espontánea.
Y ahora, podemos pensar, vale ya sabemos lo que es la estruvita, pero ¿cómo es su proceso de obtención?
Pues simplemente se introduce en un reactor de cristalización el residuo que vamos a utilizar como materia prima para extraer el N y el P (normalmente aguas residuales o digestatos obtenidos de la digestión anaerobia de residuos como el purín de cerdo) y se añade una cierta cantidad de magnesio (normalmente en forma de MgCl2 o MgO) y dependiendo del pH de la mezcla de reacción puede adicionarse una base (NaOH) para elevar el pH (8-9). Una vez que tenemos todos los componentes en el reactor, se aplica una agitación (ya sea mecánica o mediante aireación).
El Mg va entrando en contacto con el N y el P de la materia prima y poco a poco los cristales de estruvita van creciendo, según la siguiente reacción química:
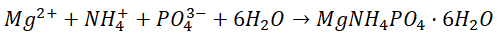
Después de aproximadamente una hora de reacción, se consigue recuperar la mayor parte de P contenido en la materia prima (y lo acompaña una cantidad equivalente de N y Mg), en forma de un cristal sólido blanquecino, la estruvita. Este sólido tiene muy buenas propiedades para ser utilizado como fertilizante, ya que la estruvita presenta una alta concentración de P y por sus características físicas (baja solubilidad), el producto puede utilizarse como un fertilizante de liberación lenta, es decir que, a diferencia de los fertilizantes tradicionales, la estruvita va liberando los nutrientes en función de las necesidades de la planta y de la etapa de crecimiento de ésta, siendo una fertilización más efectiva y evitando fenómenos de eutrofización y similares.
Existen varias tecnologías de cristalización de estruvita en el mercado (con diferentes configuraciones, tipos de reactor, morfologías, etc.), la mayoría centradas en la obtención de estruvita a partir de aguas residuales, sin embargo, en CARTIF hemos desarrollado un reactor de cristalización piloto de 50 L, intentando solventar los impedimentos técnicos que presentaban otras tecnologías. Dicho cristalizador consiste en un reactor de lecho fluidizado, es decir, la agitación de la mezcla reaccionante se consigue mediante la adición de una corriente de aire, que mantiene en suspensión los componentes de la mezcla reaccionante, facilitando su interacción y favoreciendo la formación y crecimiento de los cristales. La tecnología de cristalización de estruvita que hemos desarrollado ha sido probada en varios proyectos en los que me hemos participado, como Nutri2Cycle y Nutriman (ambos proyectos europeos del programa Horizonte2020), con resultados bastante prometedores en el proceso de cristalización (alcanzando rendimientos de recuperación de P superiores al 90%) y un buen comportamiento agronómico del producto final obtenido (estruvita).
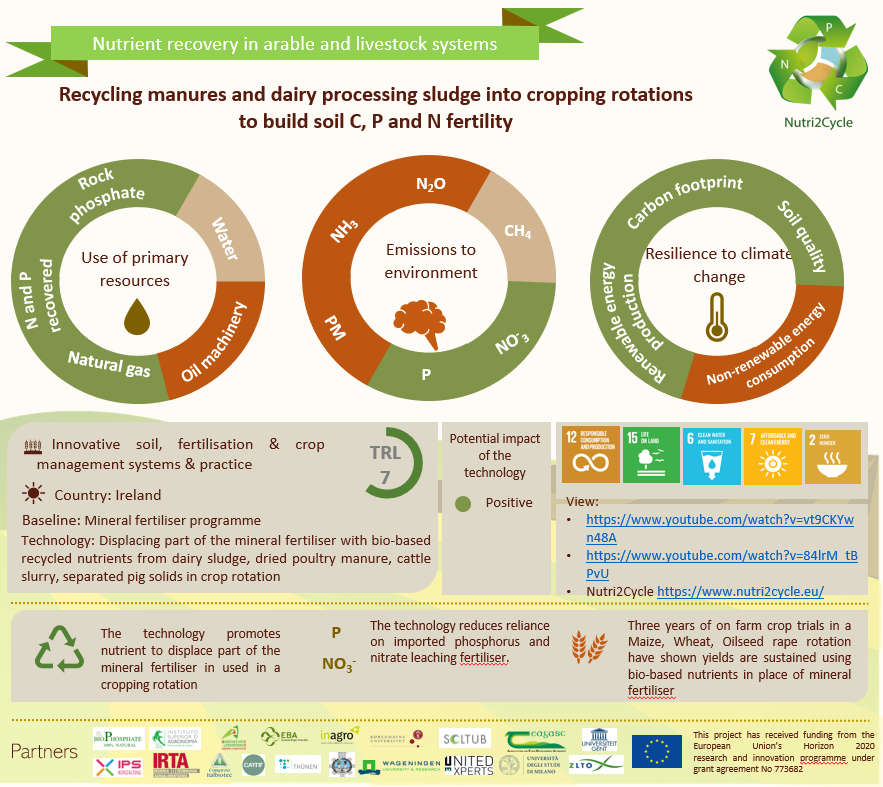
Por lo tanto, como hemos podido comprobar, gracias a las tecnologías de recuperación de nutrientes hemos desarrollado procesos sostenibles en los que valorizamos residuos (aguas residuales, digestatos, etc.) siguiendo los postulados de la Economía Circular y obtenemos un biofertilizante de origen renovable con un buen comportamiento agronómico y con características que no presentan los fertilizantes tradicionales de origen mineral no renovable (liberación lenta). Por tanto, la estruvita sería un buen candidato para sustituir o reducir la utilización de los propios fertilizantes no renovables.
En la actualidad en el Área de Economía Circular de CARTIF, seguimos trabajando en el desarrollo de esta línea de investigación y ahora mismo estamos coordinando el proyecto WalNUT (otro proyecto europeo del programa Horizonte2020), en el que junto con otros 13 socios de varios países europeos estamos desarrollando nuevas tecnologías para la recuperación de nutrientes a partir de aguas residuales (tanto urbanas como industriales). Concretamente, en el caso de CARTIF, estamos trabajando en una tecnología de recuperación de N y P mediante el cultivo de microalgas y en otra tecnología en la que los nutrientes se recuperan mediante procesos bioelectroquímicos, esta es, la tecnología de Celdas Microbianas o Microbial Fuel Cells (MFCs).
Pero si os parece, ese tema mejor lo dejamos para comentarlo en otra futura entrada del blog 😉
¡Hasta la próxima!